Kontakt:Errol Zhou (Härra.)
Tel: pluss 86-551-65523315
Mobiil/WhatsApp: pluss 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
Meil:sales@homesunshinepharma.com
Lisama:1002, Huanmao Hoone, Nr.105, Mengcheng Maantee, Hefei Linn, 230061, Hiina
Insmed on ülemaailmne biofarmaatsiaettevõte, mis on pühendunud raskete haruldaste haigustega patsientide elu muutmisele. Hiljuti teatas ettevõte, et USA toidu- ja ravimiamet (FDA) on andnud brensocatibi (endise nimega INS1007) Läbimurdelise ravimi kvalifikatsiooni (BTD) täiskasvanute mittetsüstilise fibrootilise bronhektaasi (NCFBE) raviks ja seisundi halvenemise leevendamiseks . Praegu NCFBE-le konkreetset ravi ei ole.
brensocatib on uus suukaudne pöörduv dipeptidüülpeptidaas 1 (DPP1) inhibiitor, mida töötatakse praegu välja bronhektaasi ja teiste põletikuliste haiguste raviks.
Läbimurdeline ravimite kvalifikatsioon (BTD) on uus ravimite ülevaatamise kanal, mille FDA lõi 2012. aastal, et kiirendada tõsiste või eluohtlike haiguste raviviiside väljatöötamist ja ülevaatamist, ning esialgsete kliiniliste tõendite kohaselt on ravim võrreldav olemasolevate terapeutiliste ravimitega Uued ravimid, mis võivad seisundit oluliselt parandada. BTD-ravimite hankimisel saate lähemaid juhiseid, sealhulgas FDA kõrgemad ametnikud teadus- ja arendustegevuse ajal. Uue ravimituru ülevaade on sobilik jooksvaks läbivaatamiseks ja prioriteetseks läbivaatamiseks, et tagada patsientidele uute ravivõimaluste pakkumine võimalikult lühikese aja jooksul.
FDA andis II faasi WILLOW uuringu tulemuste põhjal brensocatibi BTD. See on ülemaailmne randomiseeritud topeltpime platseebokontrolliga uuring, mis viidi läbi täiskasvanud patsientidega, kellel oli NCFBE, et hinnata brensocatibi efektiivsust ja ohutust.
Tulemused näitasid, et uuring jõudis esmasse tulemusnäitajani: kuue kuu jooksul pärast ravi oli brensocatibi ravirühma kahel annusel (10 mg ja 25 mg) märkimisväärselt vähenenud süvenemisoht 40% võrreldes platseeborühmaga (p=0,027 10 mg rühmas, 25 mg rühmas p=0,044). Lisaks jõudis uuring ka teise peamise tulemusnäitajani: platseeborühmaga võrreldes oli brensocatibi ravirühma kahel annusel (10 mg ja 25 mg) 36% (p=0,041) ja 25% (p=0,167). vastavalt kopsude ägenemise sageduse vähenemine. .
Nagu varem mainitud, tehakse uuringu täielikud tulemused teatavaks Ameerika Rindkere Seltsi (ATS) virtuaalsete kliiniliste uuringute koosolekul 24. juunil 2020.
Mittetsüstiline fibrootiline bronhektaasia (NCFBE) on tõsine krooniline kopsuhaigus, mis laieneb püsivalt infektsiooni vereringe, põletiku ja kopsukoe kahjustuste tõttu. Haigust iseloomustab sagedane kopsude halvenemine ja see vajab antibiootikumravi ja / või haiglaravi. Haiguse sümptomiteks on krooniline köha, liigne röga tootmine, õhupuudus ja korduvad hingamisteede infektsioonid, mis kõik võivad süvendada põhihaigust. NCFBE mõjutab umbes 340 000 kuni 520 000 patsienti Ameerika Ühendriikides. Praegu pole USA-s, Euroopas ja Jaapanis NCFBE-le konkreetset ravi ette nähtud
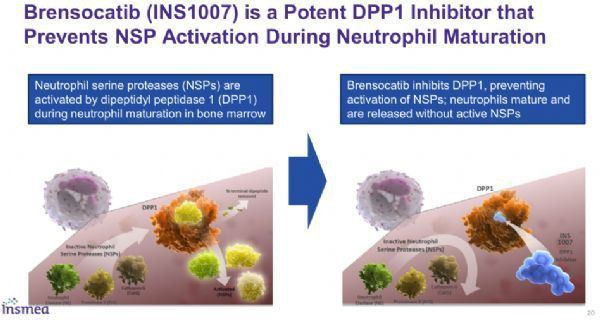
brensocatib on väikese molekuliga suukaudne pöörduv dipeptidüülpeptidaas I (DPP1) inhibiitor, mille Insmed on välja töötanud bronhoektaasi raviks. DPP1 on ensüüm. Kui luuüdis moodustuvad neutrofiilid, vastutab see neutrofiilide seriinproteaaside (NSP), näiteks neutrofiilide elastaasi aktiveerimise eest.
Neutrofiilid on kõige levinum valgevereliblede tüüp ja mängivad olulist rolli patogeeni hävitamises ja põletiku regulatsioonis. Kroonilise põletikulise kopsuhaiguse korral kogunevad neutrofiilid hingamisteedesse, põhjustades üleaktiivset NSP-d, põhjustades kopsude hävimist ja põletikku. brensocatib võib vähendada DPP1 ja selle NSP aktiveerimise pärssimisega põletikuliste haiguste, näiteks bronhektaasi kahjustusi.
Insmed loodab alustada brensocatibi III etapi projekti bronhektaasi raviks 2020. aasta teises pooles.