Kontakt:Errol Zhou (Härra.)
Tel: pluss 86-551-65523315
Mobiil/WhatsApp: pluss 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
Meil:sales@homesunshinepharma.com
Lisama:1002, Huanmao Hoone, Nr.105, Mengcheng Maantee, Hefei Linn, 230061, Hiina
Mallinckrodt on ülemaailmne professionaalne farmaatsiaettevõte, mille peakorter asub Ühendkuningriigis. Hiljuti teatas ettevõte, et USA toidu-ja Ravimihaldus (FDA) on võtnud vastu uue uimastitarbimise (NDA) terlipressiini puhul, mida kasutatakse 1. tüüpi hepatorenaalse sündroomi raviks (HRS-1). 17. märtsil käesoleval aastal teatas ettevõte, et ta on lõpetanud terlipressiin. nda jooksva esitamise. FDA on määranud retsepti narkootikumide kasutaja laadimise meetod (PDUFA) eesmärgi kuupäev september 12, 2020.
Kui see on heaks kiidetud, on terlipressiin. esimene ravim, mida kasutatakse TUNDIDES-1 täiskasvanud patsientide raviks Ameerika Ühendriikides. Varem andis FDA terlipressiini kiirõppe kvalifikatsiooni (FTD) ja harva kasutatava ravimi kvalifikatsiooni (ODD).
Hepatorenaalne sündroom (HRS) on tõsine komplikatsioon, mis esineb raske maksahaigusega patsientidel nagu tsirroos astsiit, äge maksapuudulikkus ja alkohoolne hepatiit. Hepatorenaalne sündroom tüüp 1 (HRS-1) on äge eluohtlik sündroom, mis põhjustab kiiret progresseeruva ägeda neerupuudulikkuse maksatsirroos patsientidel. Kui ravi ei ravita, on haiguse mediaanne elulemus ligikaudu 2 nädalat. suremus ületas 80% 3 kuu jooksul. Ameerika Ühendriikides, HRS-1 mõjutab 30 000 kuni 40 000 patsienti igal aastal, ja praegu ei ole heakskiidetud ravimi ravi HRS-1.
Terlipressiin on tugev vasopressiin analoog, mis selektiivselt toimib v1 retseptori silelihasrakkude väikeste arterite. Ameerika Ühendriikides ja Kanadas, narkootikumide on uuritud ravi HRS-1. Väljaspool Ameerika Ühendriike ja Kanadat on terlipressiin. heaks kiidetud kasutamiseks.
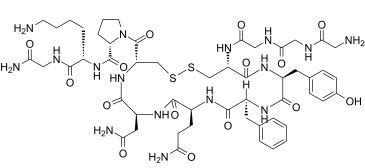
Terlipressin Keemiline struktuurivalem (Foto allikas: medchemexpress.cn)
Ravim NDA põhineb osaliselt III faasi Kinnita uuringu (NCT02770716) tulemustest. See on suurim potentsiaalne uuring (n = 300), mis on kunagi tehtud HR-1 patsientidel, ja see on tingitud terlipressiini arendamine USA ja Kanada jaoks 17 aastat. Uuringu esialgsed tulemused on välja kuulutatud 2019 American Association uuring maksahaiguste (AASLD) aastakoosolekul. Võrreldes platseebo + albumiini ravirühmaga on terlipressiini ravirühmas oluliselt pööratud neerufunktsiooni halvenemist, püsivat remissiooni ja varase neeru asendusravi (RRT) nõudlus väheneb.
Kinnita prooviversioon rakendas HRS-1 määratlemiseks rangeid kriteeriume. Tulemused näitasid, et võrreldes platseebo + albumiini ravirühmaga oli statistiliselt oluliselt suurem protsent terlipressiini + albumiini ravirühmas patsientidest, kes saavutasid kinnitatud tunni pöördumise (VHRSR). Esmane lõpp-punkt (29,1% vs 15,8%, p = 0,012). VHRSR defineeritakse järgmiselt: 2 järjestikust seerumi kreatiniinisisaldust [SCr] väärtused ≤ 1,5 mg/dL, vähemalt 2 tundi enne 14 päeva möödumist või enne seda, kui teine SCr ≤ 1,5 mg/dL, oli juhtum neeru asendusravi [RRT], ellujäämise vähemalt 10 päeva.
Lisaks näitas terlipressiin ka eeliseid nelja eelnevalt kindlaksmääratud sekundaarse tulemusnäitaja osas, sealhulgas: (1) HRS tühistamine, määratletud kui SCr ≤ 1,5 mg/dL enne 14. päeva või enne protseduuri (patsientide suhtarv: 36,2% vs 16,8%, p<0.001). (2)="" persistent="" maintain="" hrs="" reversal,="" defined="" as="" maintaining="" hrs="" reversal="" within="" 30="" days="" without="" rrt="" dialysis="" (patient="" ratio:="" 31.7%="" vs="" 15.8%,="" p=""><0.003). (3)="" hrs="" reversal="" in="" the="" subgroup="" of="" systemic="" inflammatory="" response="" syndrome="" (sirs)="" (proportion="" of="" patients:="" 33.3%="" vs="" 6.3%,="" p=""><0.001). (4)="" before="" the="" 30th="" day,="" confirm="" the="" reversal="" of="" hrs="" without="" recurrence="" of="" hrs="" (proportion="" of="" patients:="" 24.1%="" vs="" 15.8%,="" p="">

Ohutuse osas olid kõrvaltoimed sarnased 2 rühmas. 65% (n = 130) terlipressiinravi rühmas patsientidest esines tõsiseid kõrvaltoimeid ja 60,6% (n = 60) platseeborühmas. Kõige sagedasemad Tõsised kõrvalnähud on hingamispuudulikkus (10% vs 3%) kõhuvalu (5% vs 1%).
Mallinckrodt tegevjuht ja juhtiv Teadusohvitser Steven Romano, MD, sõnas: "Meil on väga hea meel, et FDA on nõustunud meie uue uimasti taotlusega (NDA), mis on oluline teetähis meie terlipressiini kliinilise arengu projektis ja mis on seotud arstide äärmiselt suure nõudlusega, neil patsientidel on ajalooliselt piiratud ravivõimalused. Ootame koostööd agentuuriga meie NDA FDA läbivaatamise ajal. "(Bioon.com)
Allikas:Mallinckrodt kuulutab välja USA toidu-ja Ravimihaldus (Fda) Uue ravimi vastuvõtmise taotlusAppRavi Terlipressiinile hepatorenaalse sündroomi raviks 1. tüüpi (HRS-1)